Mecanismos que afectan al DNA
Inhibición de ATM y DNA-Pk
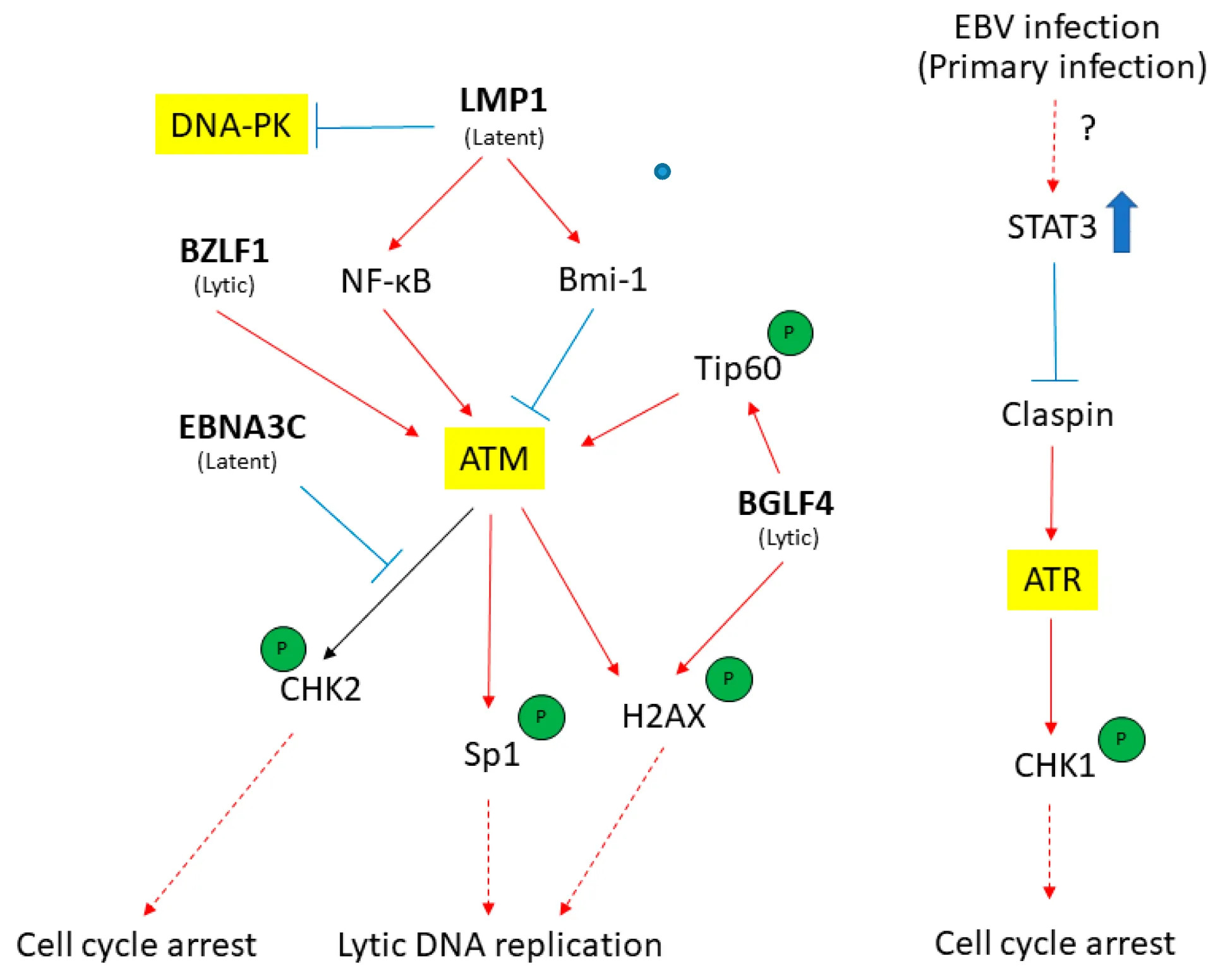
DNA-PK también es inhibida por LMP1.
Su función es reconocer el DSB e iniciar la vía de reparación NHEJ. Por lo tanto, en pacientes con EBV, está vía también está afectada directamente y la tasa de reparación de roturas de cadena disminuirá. [5]
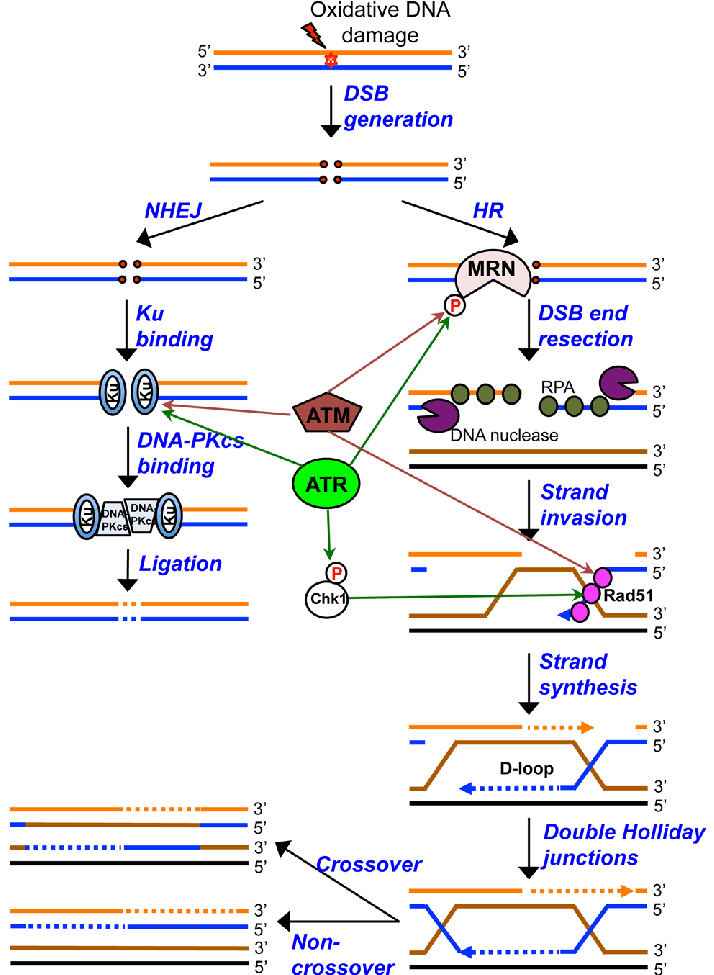
ATM es una proteína quinasa que se activa una vez el complejo MRN ha reconocido la rotura de doble cadena. Su función es activar de las vías de reparación del DNA como la mediada por recombinación homóloga o la unión de extremos no homólogos (NHEJ).
Se ha comprobado que la presencia de LMP1, una proteína viral de EBV, y la sobreproducción de BMI1 a causa de LMP1 desregula las vías de reparación. Concretamente, inhiben la producción de ATM y, por lo tanto, los pacientes presentan mayor inestabilidad genómica y un mayor riesgo de carcinogénesis. [5]
EBNA1 y lugares repetidos en tandem
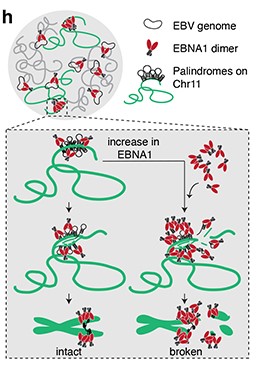
EBNA1 puede provocar DSB a lugares repetidos en tándem del cromosoma, ya que se puede asociar inespecíficamente a repeticiones que no son su diana habitual, como las que hay en el cromosoma 11 humano (más de 300 repeticiones de una secuencia de 18 nucleótidos). Esto se debe a que encuentra homología, aunque de normal se una al genoma del virus. Las secuencias del genoma humano donde se une son denominadas lugares frágiles. La abundancia de esta proteína desencadena la rotura del cromosoma, hecho que puede provocar aberraciones cromosómicas. Se ha podido comprobar la existencia de cromosomas acéntricos y/o dicéntricos a causa de EBNA1, además de la formación de micronúcleos. [6]
Por este motivo, encontrar un mecanismo para inhibir la unión de EBNA1 al cromosoma 11 podría ser un tratamiento para evitar el desarrollo de neoplasias.
EBNA1 también puede encontrar otras secuencias homólogas dispersas por el genoma humano, pero es la abundancia de la proteína en una zona concreta el hecho determinante en las roturas cromosómicas.
Inhibición de la inmunidad mediada por uracilo
Este tipo de inhibición se ha comprobado que es causada no solo por EBV, sinó también por los otros 6 virus oncogénicos que existen.
El uracilo es una base no canónica en el DNA aunque puede ser incorporada erróneamente durante la replicación o a causa de modificaciones químicas de las bases como desaminaciones dando lugar a apareamientos incorrectos (U:G). Estos se pueden solucionar por mecanismos de reparación como BER inducidos por la uracil-DNA glicosilasa, la cual elimina la base dejando un lugar apurínico (AP). El sitio AP debe ser reparado para evitar que durante la replicación, la polimerasa no sepa qué nucleótido colocar.
MMR también puede reconocer el apareamiento incorrecto U:G y repararlo.
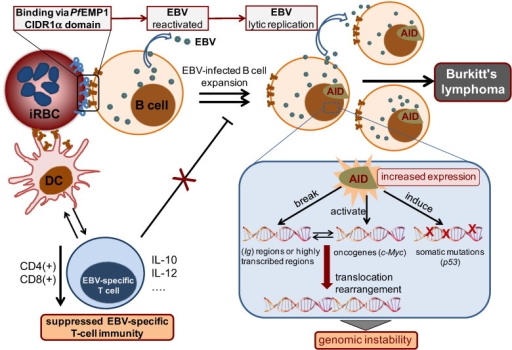
Estos mecanismos de reparación no se encuentran en el virus y, por lo tanto, la incorporación de uracilo en su genoma no puede ser reparada y esto resulta en múltiples sitios AP que, como consecuencia, dan lugar a roturas del DNA y a su degradación. El virus puede sobrevivir en la célula huésped sintetizando un antagonista de la desaminasa o simplemente inhibiendo su expresión.
No obstante, EBV ha evolucionado seleccionando las cepas que pueden sobreregular la expresión de la desaminasa, ya que no presentan tantos sitios hotstop de mutación. Esto puede ser negativo para la célula huésped, ya que la síntesis constitutiva de desaminasa no solo afecta al genoma de EBV sinó también al humano causando muchas desaminaciones de citosina a uracilo. Si los mecanismos de reparación no pueden hacer frente a tantos sitios AP, se produciran DSB e inestabilidad genómica. Las aberraciones cromosómicas derivadas pueden resultar en tumores y neoplasias. [7]